Coronavirus, cosa ha scoperto la scienza: la malattia.
Articolo del 30 Dicembre 2020
Mai era avvenuto un simile sforzo scientifico per conoscere e cercare di contrastare un virus in tempi brevi. Cosa sappiamo finora? Le risposte qui sotto, con i link alle principali pubblicazioni.
Perché si perdono gusto e olfatto?
La perdita del senso dell’olfatto e spesso del gusto, segnalata fino dai primissimi giorni e ritenuta indicativa dell’infezione perché il Sars-CoV-2 entra primariamente attraverso le mucose nasali, ricchissime di recettori Ace2, è quasi sempre temporanea. Lo suggerisce una casistica pubblicata su Jama Otolaryngology – Head and Neck Surgery da medici e ricercatori veneti e friulani insieme con alcuni colleghi britannici, relativa a 202 pazienti.
A un mese dai primi sintomi, quasi uno su due aveva completamente recuperato l’olfatto, il 40% aveva avuto un netto miglioramento e solo il 10% riferiva di non avvertire alcun cambiamento o addirittura un peggioramento. Ma questi ultimi hanno permesso di definire anche un altro elemento importante: alla persistenza del danno non corrisponde la persistenza dell’infezione.
Cosa succede al cervello?
Più passa il tempo e più si capisce che chi ha sviluppato le forme più gravi di Covid-19, quelle che hanno richiesto il ricovero e la permanenza in terapia intensiva, potrebbe avere conseguenze di tipo psichiatrico e neurologico anche a lungo termine, se già non le ha avute in ospedale. Durante le ultime settimane si sono succedute le segnalazioni soprattutto per quanto riguarda ictus e psicosi, e ora oi medici dell’Università di Liverpool, in Gran Bretagna, pubblicano, su Lancet Psychiatry, una casistica che è forse la più completa uscita finora, perché riguarda la maggior parte dei pazienti ricoverati in terapia intensiva durante il picco del mese di aprile.
In essa si descrivono 125 casi gravi: 77 hanno avuto un ictus (57 causato da un trombo, e quindi ischemico, 9 da un’emorragia e uno da un’infiammazione del cervello o encefalite), 39 sono entrati in uno stato confusionale o hanno cambiato comportamento (sette di loro avevano un’encefalite), 23 hanno risentito di un’alterazione dello stato mentale (che in alcuni era diventata una vera e propria psicosi). Non si può escludere che almeno in parte le malattie neurologiche o psichiatriche fossero preesistenti, ma neppure – come pensano in molti, tra i clinici – che il virus, in alcuni pazienti, colpisca in modo significativo il sistema nervoso, sia per fattori legati al ricovero e alle terapie (immobilità, carenza di ossigeno, farmaci, anestetici e così via) sia per una sua specifica localizzazione centrale.
Anche la Bbc ha dedicato al tema un lungo articolo, mentre il New York Times ha pubblicato un reportage dalle corsie, nel quale diversi pazienti raccontano la loro terrificante esperienza con le allucinazioni da Sars-CoV-2. Le encefaliti letargiche furono la grande, devastante eredità della pandemia di spagnola, e tra il 1918 e il 1927 colpirono cinque milioni di persone in tutto il mondo, come ha raccontato, tra gli altri, da Oliver Sacks in Risvegli.
Dopo la casistica nazionale resa nota su Brain, i neurologi dell’Università di Liverpool pubblicano ora una grande revisione dei dati internazionali che accende una nuova, inquietante luce sui possibili danni al sistema nervoso del Covid 19 e, di nuovo, chiama in causa l’encefalite letargica che funestò il mondo per vent’anni dopo la spagnola e che alcuni esperti temono possa tornare.
In questo caso gli autori hanno preso in considerazione i dati di moltissimi paesi tra i quali Italia, Stati Uniti e Cina, e hanno individuato ben 1.000 casi di conseguenze neurologiche gravi quali gli ictus e le psicosi, e poi appunto l’encefalite e altre patologie quali la sindrome di Guillain-Barré, una grave perdita della guaina protettiva delle fibre nervose causata da meccanismi non del tutto chiari ma di origine autoimmune. Fatto che spiegherebbe un altro riscontro, avvenuto in Germania, e di cui i neurologi dell’Ospedale Charité di Berlino hanno dato conto su medRxiv, pubblicazione priva di revisione: alcuni pazienti (11, nella loro casistica) hanno elevate concentrazioni di autoanticorpi diretti contro varie proteine del proprio cervello nel liquido cerebrospinale, anche quando non è possibile rilevarvi il virus. La spiegazione è che l’infezione potrebbe innescare un grave squilibrio immunitario che, dopo la fase acuta, avrebbe come esito finale una malattia autoimmune neurologica.
Come riferito dai neurologi inglesi su Lancet Neurology, comunque, ciò che è emerso è anche l’eterogeneità dei dati e le numerose lacune nei vari database: per questo – hanno sottolineato in un accorato appello gli autori – è molto importante che da ora in poi tutti i possibili effetti sul sistema nervoso vengano segnalati, descritti con cura e poi seguiti nel tempo. Per farlo si possono inserire dati e risposte dei pazienti a specifici questionari nella piattaforma studiata ad hoc.
Quali organi colpisce?
Basandosi tanto su quanto hanno visto e stanno vedendo quanto su ciò che è riportato in letteratura, i medici del Beth Israel Hospital e del Columbia University Medical Center di New York hanno pubblicato su Nature Medicine una delle più complete disamine dei molteplici effetti del Sars-CoV 2. Polmoni, cuore, cervello e sistema nervoso periferico, cuore e sistema cardiovascolare, cute, occhi, pancreas, fegato, reni, vasi: non c’è tessuto non interessato, probabilmente a causa dell’estesa infiammazione causata dal virus, al punto che tutti ritengono ormai il Covid 19 una malattia multiorgano.
Tra i gli organi nei quali si va a insediare il Sars-CoV 2 ci sono anche l’orecchio medio, insieme al mastoide (la prominenza ossea adiacente). L’hanno scoperto i medici della Johns Hopkins School of Medicine di Baltimora, che hanno riportato su JAMA Otolaryngology, Head and Neck Surgery quanto visto in due pazienti su tre. Gli autori invitano pediatri e otorinolaringoiatri alla massima prudenza in caso di procedure mediche.
Il motivo perché la malattia colpisce virtualmente quasi ogni organo e tessuto – lo si è capito presto – risiede in una proteina che tutti esprimiamo in moltissime cellule, in misura diversa da persona a persona e da tessuto a tessuto: il recettore chiamato ACE2, cui il virus si attacca per iniziare la sua invasione. E così ecco spiegati i danni (temporanei) a olfatto e gusto (di ACE 2 sono ricche le mucose nasali e orofaringee), quelli alla vista, alle fibre nervose, e poi al cuore, ai reni, al fegato, all’intestino, al pancreas, ai vasi, oltreché, naturalmente, a polmoni, bronchi e vie aeree nel loro insieme. Secondo una sintesi di 100 milioni di documenti di ogni tipo relativi al virus pubblicata su ELife, continuano ad aumentare le nuove localizzazioni della malattia.
Una disamina tra le più complete dei possibili effetti del virus è giunta pochi giorni fa da uno studio autoptico condotto dai patologi dell’Università di Gottinga, in Germania, su 27 cadaveri, pubblicato sul New England Journal of Medicine: il Sars-Cov 2 è stato rinvenuto non solo nei polmoni ma anche nel cervello, nel sangue, nel fegato, nel faringe e nei reni delle persone decedute.
Stanno poi aumentando sempre di più le segnalazioni, riassunte in un articolo di Nature, relative a un altro fatto inquietante: il coronavirus può scatenare il diabete di tipo 1, autoimmune, perché colpisce direttamente le cellule che producono insulina. Lo si è visto su pazienti, su modelli animali e su modelli in vitro.
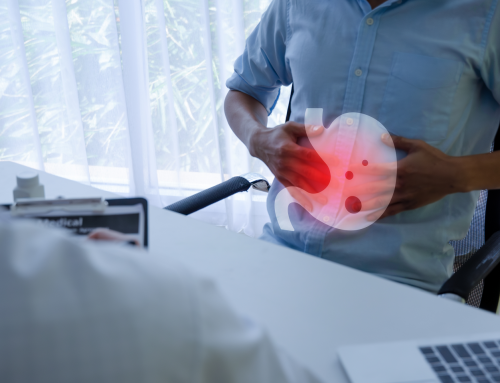
Ben nota è poi, ormai, la forma gastrointestinale, che si manifesta in un malato su tre e che è stata descritta in una casistica italiana di oltre 300 pazienti pubblicata su Clinical Gastroenterology and Hepatology.
Analogamente, tra gli organi più colpiti ci sono i reni: nell’analisi di mille pazienti ricoverati a New York , pubblicata sul British Medical Journal, il 78% dei malati arrivati in ospedale è andato incontro a gravi danni, che hanno richiesto spesso la dialisi.
Sono poi stati ormai dimostrati i danni a tutto il sistema dei vasi e al cuore (il virus può dare gravi aritmie) e persino alla cistifellea.
Cosa svelano gli organoidi
Infine, lo stesso quadro multiforme sta emergendo da numerosi studi sperimentali, condotti in quelli che vengono chiamati organoidi. Si tratta di strutture tridimensionali realizzate con cellule staminali di diverso tipo, che crescono e si differenziano grazie a un bioscheletro e a opportuni mezzi di coltura, fino a dare masse di cellule che presentano molte delle caratteristiche degli organi di riferimento. Come ha ricordato Nature in un recentissimo articolo che riassume gli ultimi risultati pubblicati, pur con tutte le cautele del caso (mancano gli effetti determinati dal fatto che nel corpo umano gli organi non sono isolati ma immersi in un contesto assai complicato) questi studi stanno confermando che il Sars-CoV 2 è in grado di infettare moltissimi distretti corporei.
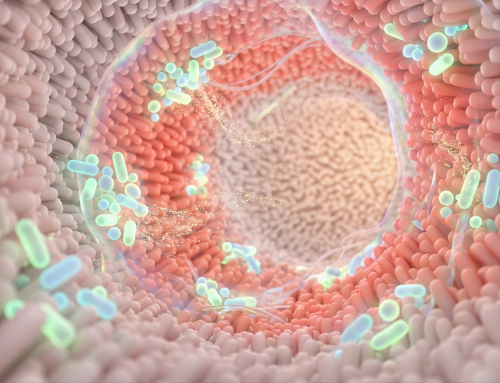
Gli organoidi hanno confermato quanto già osservato clinicamente: il Sars-CoV 2 è molto abile, quando si tratta di infettare l’intestino. I ricercatori dell’Università di Rotterdam, in Olanda, hanno pubblicato su Science quanto osservato nei loro organoidi di enterociti (le cellule intestinali). Una volta introdotto, il virus si replica in fretta e costituisce abbondanti riserve di particelle virali. Lo studio ha confermato anche, indirettamente, che gli organoidi evoluzione delle colture cellulari bidimensionali, sono un valido modello per studiare il coronavirus.
Lo stesso si è visto, del resto, con organoidi di cuore coltivati dai ricercatori del Cedars-Sinai Board of Governors Regenerative Medicine Institute, che hanno riferito su Cell Reports Medicine che il virus infetta i cardiomiociti (le cellule cardiache) e si replica perfettamente nel muscolo cardiaco, alterandone il battito dopo sole 72 ore dall’infezione. Fatto che spiega perché tanti pazienti hanno avuto pericolose fibrillazioni e patologie cardiache di diverso tipo. Non solo. Anticorpi anti ACE2 si sono dimostrati in grado di attenuare molto l’effetto del virus: anche in questo caso ACE2 è la proteina decisiva. Anche per quanto riguarda il cervello, gli organoidi hanno dato una mano a confermare le osservazioni cliniche e sperimentali.
Come riferito dai ricercatori della Johns Hopkins University di Baltimora su ALTEX, infatti, il Sars-CoV 2 infetta efficacemente le cosiddette Brain-Spheres, organoidi messi a punto 4 anni fa dalla stessa università, standardizzati e oggi considerati validi strumenti per studiare diverse patologie del sistema nervoso. In particolare il virus agisce distruggendo, con la grave infiammazione che provoca, la barriera emato-encefalica che dovrebbe proteggere il cervello, e andando a legarsi con i recettori ACE 2 presenti anche in quei tessuti.
Rischiano di più i fumatori?
Chi fuma sigarette o anche e-cig è molto più a rischio di gravi conseguenze, se contrae il Sars-CoV 2. Non solo perché i suoi polmoni sono già compromessi, e possono, più di quelli di chi non fuma, riportare conseguenze irreversibili, ma anche perché la sua coagulazione del sangue è alterata. E questo, a sua volta, ha grande influenza sui danni neurologici e vascolari tipici del Covid 19. I ricercatori dell’Università del Texas affrontano estesamente l’argomento in base a quanto osservato nei loro pazienti in uno studio pubblicato sull’ International Journal of Molecular Sciences.
Cosa fa Sars-CoV 2 al cuore?
I clinici lo hanno segnalato da tempo, e anche uno studio con risonanza magnetica, appena pubblicato su Jama Cardiology dagli specialisti dell’Università di Francoforte, in Germania, dimostra (analizzando cento casi nel dettaglio) che in tre quarti dei malati di Covid 19 c’è un serio danno cardiaco. Ma ora lo ribadiscono anche i colleghi anatomopatologi: il Sars-CoV 2 infetta direttamente il cuore. In uno studio basato su 39 autopsie di persone decedute per Covid 19, pubblicato su Jama, i ricercatori dell’Università di Amburgo hanno mostrato come il tessuto cardiaco sia invaso dal virus in sei casi su dieci. Restano da chiarire molti dettagli, soprattutto sul comportamento del sistema immunitario e delle sue citochine.
Quali eredità lascia la malattia?
Le conseguenze a lungo termine del Covid 19 dopo la fase acuta iniziano a essere più chiare, via via che si allunga il follow up di chi è guarito. Uno studio pubblicato dai medici del Policlinico Gemelli di Roma su JAMA, e condotto su 143 pazienti mostra che, a due mesi dalle prime manifestazioni della malattia, solo il 12% dei guariti è davvero tale. Un terzo continua ad avere uno o più sintomi, e più della metà ne ha 3 o più.
Negli stessi giorni, diversi altri ricercatori e clinici si sono occupati del tema, perché le conseguenze possono essere estremamente varie, come ben illustra il British Medical Journal in un dettagliato riassunto che fornisce, con tanto di disegni, anche indicazioni tanti per i medici quanto per i pazienti. Più nello specifico, si stanno moltiplicando le segnalazioni di malattie autoimmuni insorte dopo la fase acuta, spesso atipiche.
Gli specialisti del Montefiore Medical Center di New York hanno visto, su un centinaio di malati, che aumenta molto la presenza di marcatori del lupus eritematoso sistemico, forse la peggiore tra tutte le malattie autoimmuni, e che una delle conseguenze più diffuse, in chi è positivo a questi marcatori, sono i trombi, mentre quelli dell’Ospedale Garibaldi di Catania hanno riferito, sugli Annals of Internal Medicine, la storia di tre pazienti che hanno sviluppato una miastenia grave, patologia autoimmune neuromuscolare. Un po’ ovunque, oltre ai gruppi di supporto e di auto-aiuto, stanno nascendo centri clinici per seguire nel tempo questi pazienti.
Perché alcune persone si ammalano gravemente di Covid 19, e altre no?
Finalmente lo si inizia a capire, almeno per una parte di coloro che si ammalano gravemente non perché la loro salute è compromessa da altre patologie, o perché il loro sistema immunitario è lento e meno efficace a causa dell’età, ma per altri motivi finora ignoti.
La causa dell’amplissima varietà di reazioni all’infezione da Sars-CoV 2 sarebbe da ricercare, almeno in parte, nei geni e, in particolare, in alcuni di essi strettamente associati – in vario modo – agli elementi del sistema immunitario o a effetti ancora poco noti. Lo hanno dimostrato tre studi molto importanti susciti in contemporanea sulle due riviste scientifiche più accreditate, Science e Nature, nei quali ricercatori di decine di centri di ricerca e clinici, molti dei quali in Italia, hanno concentrato la loro attenzione sul genoma dei malati più gravi, per capire se ci fosse qualcosa di specifico. Il coordinatore dei primi due è Jean-Laurent Casanova, ricercatore dell’Howard Hughes Medical Institute della Rockefeller University, che a febbraio ha iniziato a raccogliere i campioni dei malati che stavano peggio con l’intenzione di controllare l’espressione di 13 geni associati alla risposta ai virus influenzali e, in particolar modo, alla produzione di interferoni, molecole che l’organismo utilizza con antivirali e antinfiammatori naturali. L’obbiettivo era trovarne 500, ma in agosto ce n’erano già 1.500, e oggi si va per i 3.000. Come riferito nel primo articolo, 23 dei 659 pazienti studiati (cioè il 3,5% del totale) aveva un difetto proprio nell’espressione di interferoni. Ciò spiega perché queste persone possano difendersi in modo meno efficiente dal coronavirus.
Questa scoperta, però, ha suggerito a Casanova di cercare anche in un’altra direzione: l’autoimmunità. E’ noto infatti da tempo che in alcune malattie autoimmuni, nelle quali cioè la produzione di anticorpi è rivolta verso lo stesso organismo, ci sono anche autoanticorpi contro gli stessi interferoni. Nel secondo studio, quindi, i ricercatori hanno controllato la presenza di questi autoanticorpi in 987 pazienti, e li hanno trovati in 101, per lo più (nel 94% dei casi) di sesso maschile. Tutto ciò ha diverse conseguenze. Innanzitutto si potrebbero analizzare tutti coloro che si ammalano con sintomi per verificare qual è il loro assetto genetico e avere quindi una prognosi precisa dell’evoluzione della malattia, nonché la possibilità di definire per tempo un piano di cura personalizzato.
Poi ci sono fondati motivi per controllare, nell’ambito di studi clinici ad hoc, le terapie che agiscono sugli interferoni: ne esistono già diverse utilizzate nel campo dell’autoimmunità, così come esistono singoli interferoni che potrebbero colmare le carenze dovute ai geni: se ne conoscono 17 diversi, alcuni dei quali somministrabili per via iniettiva. Un’altra possibilità è la plasmaferesi, una sorta di filtraggio del plasma con il quale si sottraggono appunto al plasma gli autoanticorpi presenti. Un ulteriore tassello, poi, è quello fornito dal terzo studio, uscito su Nature, che ha portato a una scoperta sorprendente: una parte di chi è più suscettibile all’infezione deve la sua maggiore vulnerabilità a geni che appartenevano all’uomo di Neanderthal o di Denisovan o più probabilmente a ibridi tra i due, che abitavano nell’Europa del Sud tra i 50 e i 60.000 anni fa.
Questa volta i coordinatori sono i ricercatori della Human Evolutionary Genomics Unit della Okinawa Institute of Science and Technology Graduate University (OIST) giapponese insieme a quello del Max Plank Institute di Leipzig, in Germania, guidati da Svante Paabo, uno dei massimi esperti mondiali di paleogenetica e paleoantropologia, che hanno concentrato la loro attenzione sul cromosoma 3. Nell’ambito della COVID-19 Host Genetics Initiative, infatti, hanno analizzato quello di oltre 3.100 malati con Covid 19 in diversi livelli di gravità, e trovato che chi possiede un lungo frammento (di poco meno di 50.000 basi) che arriva direttamente dagli antenati neanderthaliani, e, in particolare, una tra le sue 13 possibili varianti, è destinato a stare peggio di chi non ha le stesse varianti.
Per i primi, infatti, il rischio di aver bisogno della ventilazione assistita è triplo rispetto ai secondi, e molti indici sono peggiori. Non si sa esattamente in che modo questo frammento di DNA influenzi la sensibilità all’infezione da Sars-CoV 2, ma si sa, per esempio, che è praticamente assente in Africa e nelle popolazioni che vivono in estremo oriente, mentre in quelle dell’oriente meridionale è presente in un abitante su due, e in Europa nel 16% della popolazione. E si sa che questo trova riscontro nella gravità della malattia nelle stesse zone. Ora i ricercatori stanno cercando di capire perché questi geni preistorici siano così importanti, ed eventualmente come intervenire in chi li ha nel suo genoma.
Fonte: Lab24 de IlSole24Ore