Coronavirus, cosa ha scoperto la scienza: vaccini e farmaci.
Articolo del 30 Dicembre 2020
Mai era avvenuto un simile sforzo scientifico per conoscere e cercare di contrastare un virus in tempi brevi. Cosa sappiamo finora? Le risposte qui sotto, con i link alle principali pubblicazioni.
Quali farmaci si stanno dimostrando più promettenti?
Al momento una terapia antivirale specifica per l’infezione da Sars-CoV-2 non esiste. Recentemente anche grazie all’aumento delle conoscenze, sono però stati messi a punto percorsi di trattamento (solo su indicazione medica) sia a domicilio per i casi più lievi sia in ospedale quando è necessario il ricovero. Nel primo caso, oltre all’idratazione e al proseguimento di eventuali terapie croniche, l’Agenzia Italiana del Farmaco (AIFA) consiglia l’impiego di antinfiammatori non steroidei (FANS) per il controllo del sintomi, così come il paracetamolo.
In casi specifici, il medico può indicare un trattamento con eparina o derivati del cortisone che possono essere impiegati in particolare quando sia richiesta ossigenoterapia a domicilio. Non viene invece consigliato l’impiego di antibiotici, idrossiclorochina o antivirali per il virus HIV.
Nel trattamento ospedaliero, invece, viene confermata in specifici pazienti l’utilità di desametasone in caso di ossigenoterapia di supporto, sulla scorta dei risultati degli studfi RECOVERY e SOLIDARITY: il farmaco ha dimostrato di ridurre di un terzo la mortalità dei pazienti in ventilazione assistita. Le eparine possono essere somministrate sia in forma profilattica che sotto l’aspetto della terapia: in questo secondo caso occorre valutare le caratteristiche del paziente per l’impiego a dosaggi più elevati.
L’unico antivirale che ad oggi ha dato risultati è Remdesivir, nato per il trattamento dell’infezione da Ebola. Tuttavia il farmaco, sempre secondo AIFA; non può essere considerato uno standard di cura, pur se in alcuni studi ha dimostrato di ridurre il ricovero e le complicanze. Secondo AIFA l’impiego del farmaco è indicato in casi specifici e l’OMS ha formulato una raccomandazione negativa debole sull’impiego del farmaco nell’intera popolazione dei pazienti ricoverati.
Tra i trattamenti in fase avanzata di studio va ricordata la terapia con baricitinib, sulla scorta dei risultati di uno studio pubblicato su New England Journal of Medicine, che ha portato all’autorizzazione all’uso di emergenza della Food and Drug Administration (FDA) per baricitinib insieme a remdesivir in specifiche popolazione di pazienti.
A che punto sono gli anticorpi monoclonali?
L’attenzione della scienza si concentra sugli anticorpi monoclonali oltre che su altre molecole. E si affaccia anche la possibilità di impiegarli in chiave preventiva, stando a quanto riporta un’ipotesi di lavoro tra UCLH e AstraZeneca, che avrebbero messo a punto un insieme di anticorpi che potrebbero avere un senso nei soggetti esposti all’infezione, con azione preventiva.
Per il resto, gli studi si sviluppano su strade diverse: si va da possibili cure antivirali che agiscano su specifici meccanismi che possano inibire una fase chiave del passaggio del virus, dalla sua “entrata” nelle cellule fino alla possibilità di “ricostruire” il patrimonio genetico e alla “liberazione” nell’organismo. per duplicarsi e continuare nella sua invasione.
Secondo Stefano Vella, docente di Salute Globale all’università Cattolica di Roma, “probabilmente occorrerà usare una combinazione di farmaci per bloccarne l’entrata, oppure usare anticorpi monoclonali, magari attaccando le proteasi, enzimi che il virus impiega per uscire dalle cellule che infetta e invaderne altre”.
Proprio sul fronte degli anticorpi monoclonali c’è grande attesa, anche per la ricerca italiana: recentemente è stata pubblicata su BioxRiv uno studio su MAD0004J08, un anticorpo monoclonale particolarmente potente che ha la capacità di legare la proteina Spike e inattivare il virus, messo a punto dal Monoclonal Antibody Discovery (MAD) Lab di Fondazione Toscana Life Sciences
Per il resto sono in fase 3 Vir Biotechnology e GlaxoSmithKline, mentre le americane Regeneron (azienda che ha sviluppato gli anticorpi che hanno curato Trump) ed Eli Lilly, stanno portando avanti i processi di registrazione per i loro candidati. Infine, è in studio un anticorpo monoclonale specifico per il virus, che lega la proteina S virale, attualmente in fase di sperimentazione iniziale sull’uomo. Si punta anche ad agire su una specifica proteasi dei coronavirus che in qualche modo agirebbe come “chiave” per far entrare il virus all’interno delle cellule polmonari.
L’obiettivo è TMPRSS2, un enzima presente nel corpo umano, utilizzato dal virus come un vero e proprio “piede di porco” per accedere nelle cellule a replicarsi, su cui potrebbero agire anche farmaci già esistenti.
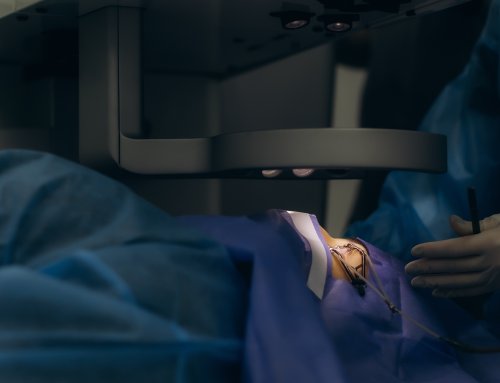
A che punto sono i vaccini?
La campagna di vaccinazione europea e italiana è iniziata, grazie a un’approvazione condizionata di EMA e AIFA, che ha la durata di un anno, per il vaccino di Pfizer/BionTech. Quella di Moderna è invece attesa per gennaio, dopo il via libera Fda per gli Stati Uniti. Al momento l’indicazione prevede che possano essere somministrati a tutte le persone con più di 16 anni, senza particolari restrizioni.
Entrambi i vaccini sono basati sulla somministrazione del materiale genetico (RNA) della proteina spike, ed entrambi hanno mostrato una grande efficacia nel prevenire lo sviluppo dei sintomi.
Ma restano da chiarire molti aspetti. I principali riguardano la durata della protezione, la prevenzione della diffusione del virus dalle persone vaccinate oltreché quella dello sviluppo della malattia, la diversa efficacia in popolazioni specifiche quali i bambini, gli immunodepressi, le donne in gravidanza, le persone con altre malattie e così via, oltre a una visione più esaustiva della sicurezza, che sembra per ora molto elevata. Per alcune di esse inizia a esserci qualche dato ma, soprattutto, sono in programma studi specifici.
Moderna ha iniziato dagli anziani, perché sono loro le vittime principali della malattia. Una prima pubblicazione del New England Journal of Medicine, relativa a soli 40 soggetti, ha concluso che il vaccino è sicuro anche dopo i 70 anni. Negli stessi giorni l’azienda ha annunciato l’avvio della sperimentazione sui ragazzi: ne sta arruolando 3.000, di età compresa tra i 12 e i 18 anni.
Per quanto riguarda la sicurezza, nelle prime settimane di inoculazione del vaccino Pfizer in Gran Bretagna e Stati Uniti, i casi di allergie gravi sono stati pochissimi e secondo un articolo pubblicato su Science le reazioni sarebbero da attribuire a una delle sostanze utilizzate per sciogliere l’RNA: il polietileglicole o PEG, in nanoparticelle (cioè in particelle il cui diametro medio è di qualche milionesimo di millimetro), usatissimo in prodotti di impiego quotidiano (per esempio negli shampoo e nei dentifrici), e contenuto anche in quello di Moderna. Ci potrebbero essere infatti soggetti che, esposti in passato al PEG, avrebbero sviluppato una reazione allergica, e che ora, entrando nuovamente in contatto con la sostanza, avrebbero avuto una reazione più grave, anafilattica, ma sempre curabile. Ma mancano prove definitive e, nel frattempo, si sta cercando attivamente di capire che cosa, in alternativa al PEG, potrebbe scatenare l’allergia.
Il vaccino AstraZeneca/Oxford/IRBN, basato su un approccio diverso, cioè sull’inserimento del DNA della proteina spike in un vettore virale (un virus disattivato di primate), che sembrava molto vicino al traguardo, potrebbe in realtà arrivare con qualche mese di ritardo.
La sperimentazione di fase 3, condotta contemporaneamente in Brasile, Sud Africa e Gran Bretagna, è stata infatti condizionata da un errore di dosaggio: in uno dei bracci la dose impiegata è stata la metà di quella prevista. Ciò ha permesso di scoprire, per serendipità, quindi per caso, che il protocollo andava corretto, e cioè che l’efficacia migliore, attorno al 90% (contro il 62% rilevato nei bracci “giusti”), si otteneva somministrando mezza dose alla prima inoculazione, e una dose intera alla seconda.
Tutto ciò ha sollevato molte critiche e dubbi della comunità scientifica internazionale, che in diverse sedi si è espressa sottolineando che dati provenienti da protocolli diversi adottati nei paesi coinvolti non possono essere assimilati e compresi in un’unica valutazione statistica, e che l’efficacia più alta è vista, per ora, solo in una piccola percentuale di pazienti. Non solo. Secondo un’indagine del New York Times l’azienda anglo-svedese ha stipulato accordi per la produzione per il mercato asiatico con un’azienda cinese, la Kangtai Biological Products, sulla quale gravano accuse pesantissime quali quella di aver prodotto un vaccino errato contro l’epatite B, che nel 2013 avrebbe causato la morte di 17 bambini e prima, nel 2004, un vaccino inefficace contro la rabbia, che in quell’anno aveva già ucciso 2.600 persone.
Negli ultimi giorni, poi, l’azienda ha annunciato, senza fornire dettagli, un’altra decisione che ha suscitato non poche perplessità: quella di partire con una sperimentazione nella quale il suo vaccino sarà dato insieme allo Sputnik V, il vaccino dell’Istituto russo Gamaleya, sugli effetti e sulla sicurezza del quale non esiste alcuna pubblicazione scientifica, ma solo un comunicato del fondo d’investimento statale che ha finanziato la ricerca. L’idea è quella di potenziare l’effetto, visto che l’approccio è identico e che cambiano solo i vettori virali. Ma la storia dei vaccini è costellata di imprevisti, i vettori virali sono stati talvolta al centro di incidenti anche gravi, e in un momento in cui c’è poca chiarezza su questo vaccino, unirne un secondo di cui si sa pochissimo è considerata da molti una decisione fuori luogo.
Forse anche in conseguenza di questo caos l’azienda a metà dicembre ha annunciato di voler sospendere, per ora, la parte di studio in programma su 3.000 bambini inglesi di 5 anni di età.
Gli ultimi dati, pubblicati su Lancet, sono relativi alla sicurezza e mostrano che la popolazione anziana, con più di 70 anni (240 i soggetti studiati) , sarebbe meno suscettibile agli effetti collaterali rispetto a quella più giovane.
Anche per Johnson & Johnson e la sua affiliata Janssen, specializzata in vaccini, è giunto il momento della fase 3: lo studio ENSEMBLE ha appena terminato l’arruolamento di oltre 45.000 persone in diversi paesi, pronte a ricevere l’unica somministrazione di un preparato basato su un vettore virale che contiene il DNA della spike.
I dati dovrebbero essere resi noti entro fine gennaio, e se saranno positivi le approvazioni saranno chieste entro febbraio.
Il vaccino GlaxoSmithKline-Sanofi, basato su un approccio più tradizionale, e cioè sulla somministrazione di una porzione della proteina spike già formata più uno stimolante, ha invece subito una battuta d’arresto. I dati della sperimentazione di fase 3 hanno infatti mostrato un’efficacia che, sebbene ritenuta sufficiente da molte agenzie regolatorie, è considerata insoddisfacente dalle due aziende, soprattutto nella popolazione con più di 60 anni, che avrebbe risposto positivamente nel 62,5% dei casi, contro l’89% del gruppo delle persone con 18-49 anni, e l’85% di quelle di età compresa tra i 50 e i 59 anni.
I nuovi test inizieranno a partire dal prossimo mese di febbraio.
La partnership prevede che Sanofi sintetizzi la sezione di proteina, e GSK fornisca l’adiuvante che, in questo caso, è lo squalene, una sostanza ancora oggi ottenuta dal fegato degli squali, e già usata per molti altri vaccini. Come ha ricordato la BBC in un lungo articolo dedicato al tema, gli adiuvanti sono indispensabili per questo tipo di vaccini, anche se non è del tutto chiaro perché. Ma, curiosamente, sono ancora ottenuti, nella stragrande maggioranza dei casi, da fonti naturali come appunto le squalene (un’altra grande famiglia è quella delle saponine, ottenute da un albero cileno), fatto che potrebbe rallentare la sintesi di miliardi di dosi anche per questo vaccino, qualora si riuscisse a definire una dose ottimale.
GSK sta collaborando anche con la canadese Medicago, che studia un vaccino basato su un approccio diverso: quello delle cosiddette virus-like particles, o VLP, ossia particelle virali sintetizzate in laboratorio che imitano quelle vere senza però causare la malattia, e che dovrebbero quindi stimolare una risposta immunitaria più efficace, perché diretta contro più di una proteina. Anche in questo caso sono previsti adiuvanti. Nei giorni scorsi è stato annunciato l’avvio della sperimentazione di fase 2/3 su diverse fasce d’età, compresi gli over 65, per un totale di circa 30.000 persone coinvolte.
C’è un vaccino che aveva suscitato speranze ma che, al contrario, non diventerà mai tale: quello australiano chiamato UQ-CSL, sviluppato con l’Università del Queensland e di cui il governo aveva già prenotato 51 milioni di dosi. La sperimentazione è stata interrotta perché, come ha riferito Science, il vettore virale utilizzato, che conteneva frammenti del virus HIV (per aumentare la stimolazione), causa anche la formazione di anticorpi diversi da quelli anti Sars-CoV 2, e questo impedisce di valutarne la reale efficacia. Il fatto non deve stupire: è stato calcolato che, in media, la percentuale di medicinali che passano dalla fase 1 alla 2 sia di poco superiore al 60%; tra la 2 e la 3 il tasso scende al 30% e da quest’ultima alle prime approvazioni risale al 58%. I vaccini non fanno eccezione, perché in media solo il 16% arriva sul mercato, e anche se in questo caso sono state messe in campo forse eccezionali, sicuramente diversi tra quelli in corsa non vedranno mai la luce.
La Cina, come la Russia, ha sviluppato i suoi vaccini in modo autonomo, e iniziato a vaccinare la popolazione a rischio tra cui i militari prima della conclusione della fase sperimentale. I suoi prodotti sono tre: due sviluppati dal China National Biotec Group (CNBG), statale, e uno dalla Sinovac Biotech, azienda privata. Quest’ultima ha annunciato di aver iniziato il reclutamento di 20.000 persone per la fase 3, e per il momento ha pubblicato quelli della fase 1-2 su Lancet. Il suo vaccino è basato su vettori virali, che sono però risultati associati a un tasso di effetti collaterali piuttosto alto, del 9%.
I due vaccini statali Sinopharm sono invece costituiti da virus inattivati, che inducono una forte reazione perché contengono altre proteine immunogeniche oltre alla spike, e sono entrambi in fase 3: saranno sperimentati su poco meno di 30.000 soggetti in vari paesi.
Altre decine di vaccini sono in studio e molti di essi sono già nelle fasi 1 e 2 della sperimentazione clinica. Vari siti seguono giorno per giorni l’evoluzione delle notizie; tra gli altri c’è quello di Reuters, che aggiorna anche sulle ordinazioni dei diversi paesi.